美国FDA公示 | 诺唯赞司美格鲁肽中间体FDA DMF备案成功!
2025-02-10
近日,诺唯赞成功完成司美格鲁肽中间体(生物重组法制备)【备案名称:ARG34GLP-1(9-37)】在美国食品药品监督管理局(FDA)的药品主文件(DMF)备案(DMF NUMBER ASSIGNED:40502)。使用诺唯赞相关产品的客户在FDA递交药品申请时只需直接引用DMF备案信息即可代替申报过程中需要提供有关原料和辅料的具体信息,从而简化评审流程,提高审批效率。这意味着诺唯赞产品在美国市场的商业化进程迈入了新阶段。

关于司美格鲁肽:
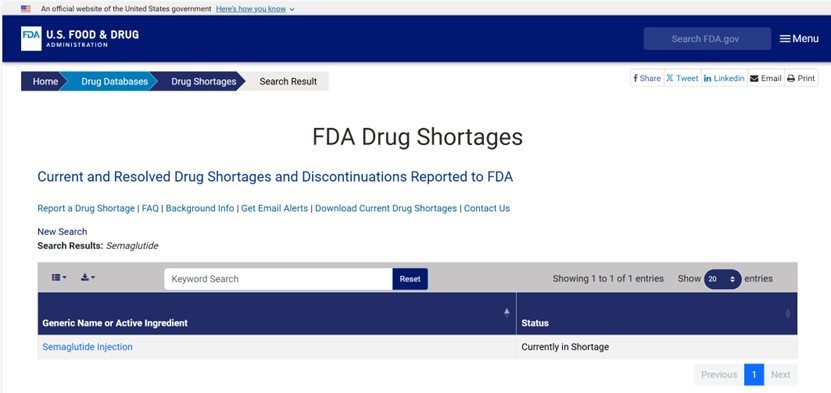
司美格鲁肽(Semaglutide),也被称为索马鲁肽,是诺和诺德公司继利拉鲁肽之后开发的第二代GLP-1受体激动剂,也是全球首个可同时用于皮下注射和口服制剂的GLP-1RA,主要用于2型糖尿病的治疗,同时在以2型糖尿病为基础衍生的心血管疾病、肥胖症、非酒精性脂肪肝病、神经系统性疾病等多种疾病上被批准使用于临床。由于其不良反应发生概率低,提高了患者用药的依从性与便利性,在药物经济学体现出明显的优势。自2017年在美国上市以来,成为当前备受瞩目的肽类药物之一,2023年全球销售额212亿美金,2024前三季度全球销售额达203亿美元,由于市场需求还在增长,目前仍保留在《FDA短缺药品目录》中。
关于DMF:
药物主文件(Drug Master File, DMF)是一份提交给美国FDA的保密文件,内容包括产品的制造商、产品属性、生产工艺、检验方法、杂质研究、包装储存、稳定性等方面的资料和数据。DMF认证的核心是确保药品原料的产品安全、质量可靠、生产流程符合规范并符合美国FDA的相关要求。
关于诺唯赞:诺唯赞司美格鲁肽供应链解决方案
扩产能、降成本、协同打造新质生产力
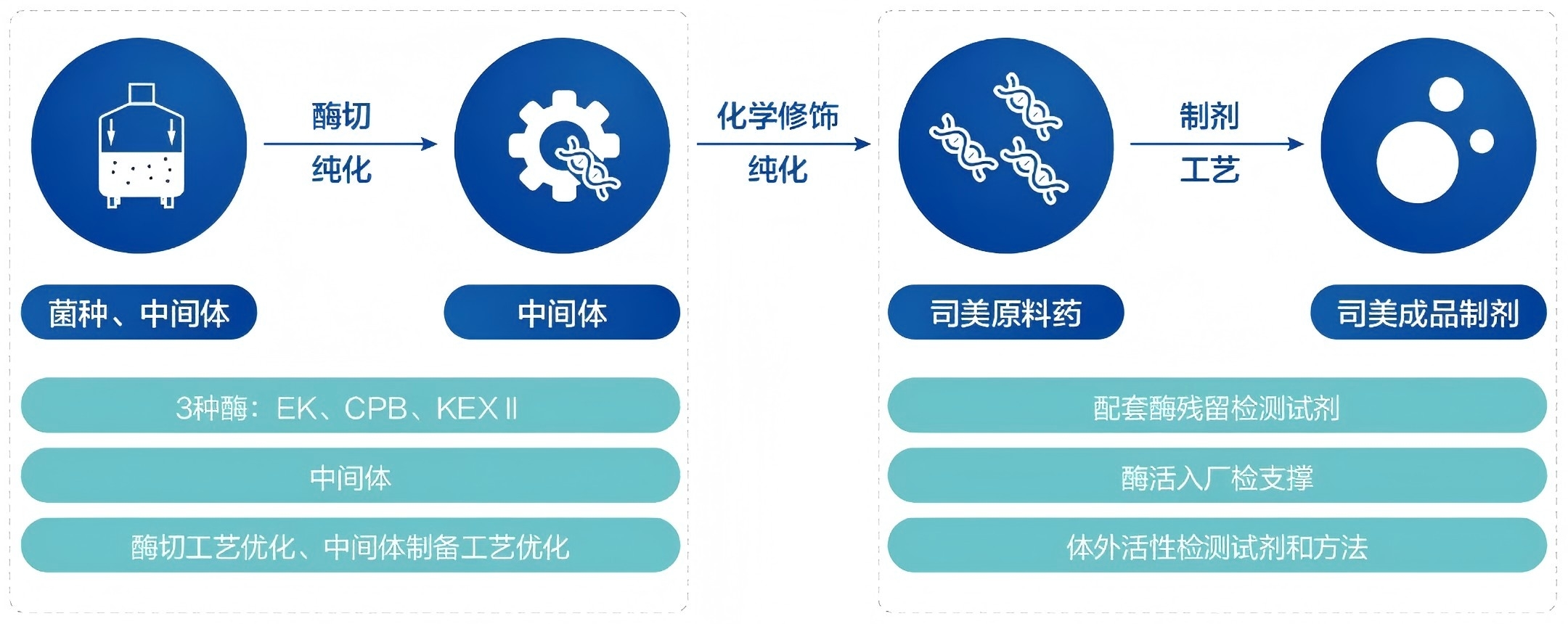
生物法核心
缩短中间体工艺开发周期、提高收率、降低成本

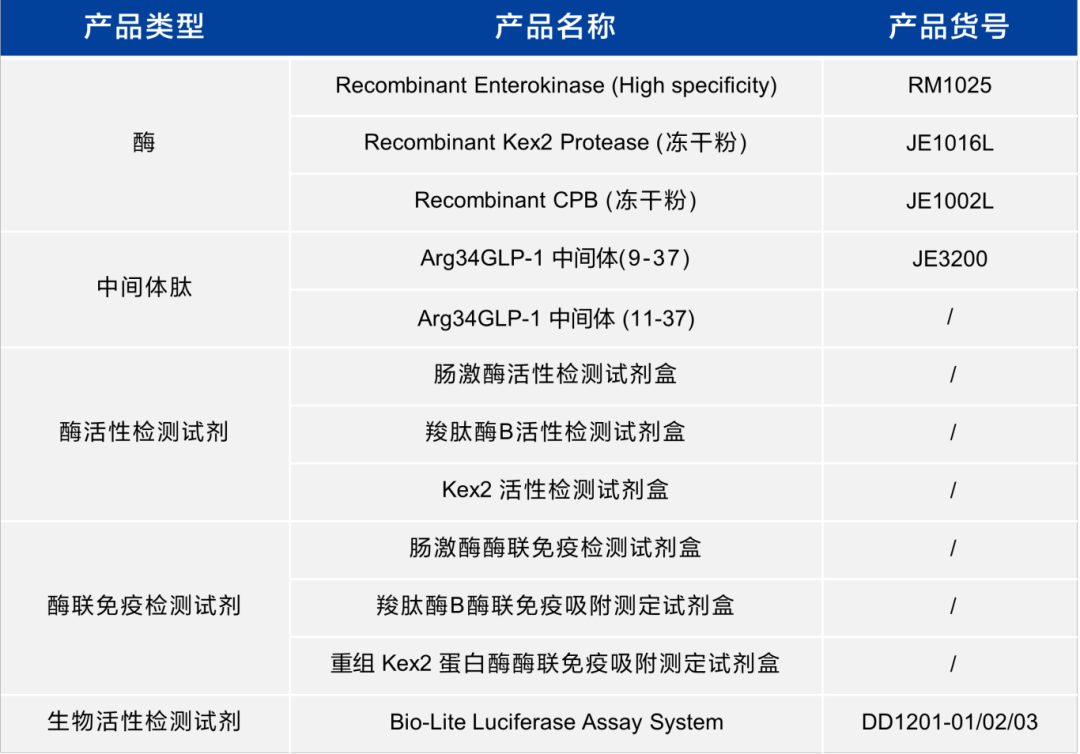
相关产品列表